Tolong jawabannya ya makasihh INI JAWABAN TERBAIK Perbedaan senyawa ion dan senyawa kovalen. Senyawa ionik terbentuk oleh transfer elektron yang bermuatan.

Ikatan Kovalen Polar Dan Nonpolar Penjelasan Perbedaan Dan Contoh
Ikatan Kovalen Nonpolar.

. Ikatan Kovalen Non Polar. Senyawa kovalen tidak memiliki kemampuan ini karena mereka tidak mengandung ion. Hal ini karena air melarutkan zat polar yang merupakan konsistensi senyawa ionik sedangkan senyawa kovalen non-polar.
Contoh ikatan kovalen non polar. Ikatan kovalen nonpolar adalah ikatan kovalen yang terbentuk ketika atom membagikan elektronnya secara setara sama. Senyawa tersebut terbentuk karena unsur-unsur saling berikatan.
Karena PEI tertarik sama kuat maka bentuk molekul pada senyawa F 2 adalah simetris. Atom N pada molekul amonia NH3 mempunyai satu. Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas.
Untuk senyawa karbon Mr sama rantai C memanjang titik didih rantai bercabang bulat Perbedaan Senyawa Polar dengan Non Polar. Pada senyawa kovalen yang memiliki lebih dari dua unsur kepolarannya ditentukan oleh beberapa hal berikut ini. Dapat larut dalam air.
Ikatan kovalen koordinasi hanya dapat terjadi jika salah satu atom mempunyai pasangan elektron bebas PEB. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya. Ikatan yang terjadi antara ion-ion logam dan non logam Ikatan terbentuk akibat gaya tarik listrik antara ion yang berbeda Ikatan ion juga dikenal sebagai ikatan elektrovalen.
Jadi ikatan kovalen ini syaratnya ada molekul yang atom pusatnya mempunyai pasangan elektron bebas PEB. Perlu diingat baik-baik. Senyawa kovalen tidak dapat menghantarkan listrik.
Pada contoh ikatan kovalen polar yaitu pada molekul HCl pasangan elektron ikatan PEI cenderung tertarik ke salah satu atom yang memiliki elektronegativitas lebih besar yaitu atom Cl oleh karena itu bentuk molekulnya mengutub pada atom Cl sehingga menjadi asimetris tidak simetris. Biasanya terjadi ketika ada atom mempunyai afinitas elektron yang sama atau hampir sama. Hal ini terjadi karena antara dua atom F dan F memiliki keelektronegatifan yang sama besar atau perbedaan elektronegativitas adalah nol.
Ketika kita pertama kali tahu tentang kimia sebagian besar dari kita menemukan itu menyenangkan dan menarik. Ikatan kovalen koordinasi adalah ikatan yang terjadi jika pasangan elektron yang dipakai bersama hanya berasal dari satu atom saja sedangkan yang lain tidak menyumbangkan elektron. Jika momen dipol tidak sama dengan 0 senyawa kovalen tersebut merupakan senyawa kovalen polar.
HF HCl dan HBr. Sebuah atom berfungsi sebagai pemberi pasangan. Bila sama-sama polarnon polar yang Mr besar titik didihnya lebih besar.
Semakin dekat nilai afinitas elektron maka semakin kuat ikatannya. Misalnya pada senyawa HF dimana elektron bersamanya digunakan secara tidak seimbang oleh kedua inti atom H dan inti atom F. Senyawa ion juga lebih larut dalam air dibandingkan senyawa kovalen.
Ikatan Kovalen Nonpolar terjadi jika pasangan electron yang dipakai bersama tertarik ke semua atom yang berikatan. Perhatikanlah gambar berikut ini. Ikatan antara unsur-unsur ini beragam bergantung pada jenis unsur.
Senyawa kovalen koordinasi adalah ikatan kovalen di mana pasangan elektron yang dipakai bersama hanya disumbangkan oleh satu atom sedangkan atom yang satu lagi tidak menyumbangkan elektron. HF asam florida. Tapi kemudian menjadi membosankan ketika Anda bertemu dan belajar sifat-sifat kimia ikatan kimia tabel unsur dan seterusnya dan sebagainya.
Pada senyawa kovalen di samping itu elektron bersama oleh beberapa atom. Senyawa kovalen berwujud lunak dan tidak mudah rapuh. Senyawa-senyawa kovalen dengan ikatan kimia dengan kovalen nonpolar maka tidak ada muatan parsial baik positif maupum negatif dalam molekul-molekul tersebut.
H2 N2 F2 2 Pasangan Elektron Bebas PEB Atom pusat memiliki pasangan elektron bebas PEB. Ikatan kovalen nonpolar terjadi pada molekul. Perbedaan Ikatan Kovalen Polar Ikatan Kovalen Nonpolar 1 Keelektronegatifan Terdapat perbedaan keelektronegatifan.
Kedua inti atom yang menarik electron valensi adalah sama besar. Sebutkan 8 Perbedaan Senyawa Polar dan Nonpolar. Senyawa kovalen memiliki ikatan kovalen.
Pada senyawa ionik elektron diberikan dari atom dari satu unsur ke unsur lainnya. Senyawa Kovalen Polar dan Non-Polar Ikatan Kimia Bentuk Molekul dan Interaksi Antarmolekul. Tidak terdapat perbedaan keelektronegatifan.
Jumlah atom 2 harus berbeda. Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas. Memiliki pasangan elektron bebas bentuk tdk simetris Berakhir ganjil kecuali BX3 dan PX5.
Dapat terbentuk apabila unsur-unsur yang bereaksi mempunyai perbedaan daya tarik elektron yang cukup besar Perbedaan yang besar memungkinkan terjadi serah-terima. Ikatan ion membentuk senyawa ion sedangkan ikata kovalen membentuk senyawa kovalen. Jelaskan perbedaan antara senyawa kovalen polar dengan kovalen nonpolar.
Senyawa kovalen polar dalam bentuk larutannya dapat terionisasi sempurna atau terionisasi sebagian menjadi ion. Ikatan ini terjadi pada atom atom yang homointi. Sebuah senyawa terjadi ikatan kovalen polar apabila ada perbedaan kelektronegatifan yang mengakibatkan terjadinya pengutuban muatan.
Senyawa kovalen memiliki titik didih dan titik leleh yang rendah. Senyawa kovalen tidak larut dalam pelarut polar namun larut dalam pelarut organik. Kita merasa frustrasi harus menghafal sifat.
Sehingga sebaran muatan electron di antara kedua inti atom yang berikatan homogen. Senyawa kovalen bersifat polar apabila dilarutkan kedalam air karena air merupakan pelarut polar. Kepolaran pada molekul ini terjadi karena antara atom H dan atom Cl memiliki perbedaan.
Antara molekul air dan molekul zat terlarut akan terjadi tarik menarik yang cukup kuat untuk memutuskan ikatan-ikatan molekul tertentu dan membentuk ion. SEORANG PENGGUNA TELAH BERTANYA Jelaskan perbedaan antara senyawa kovalen dan senyawa ion serta berikan contohnya. Secara garis besar ikatan antar unsur dibedakan menjadi dua jenis yaitu ikatan logam dan ikatan kovalen.
Berdasarkan kepolarannya senyawa kovalen terbagi menjadi senyawa kovalen polar dan senyawa kovalen non polar. Jika jumlah momen dipol 0 senyawa kovalen tersebut merupakan senyawa kovalen nonpolar.

Jelaskan Perbedaan Antara Senyawa Polar Dengan Nonpolar Dan Berikan Masing Masing Contohnya Brainly Co Id
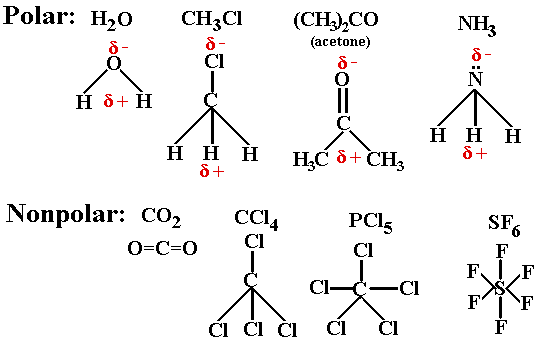
4 Perbedaan Ikatan Kovalen Polar Dan Non Polar Materi Kimia

Perbedaan Polar Dan Nonpolar Apayangdimaksud Com
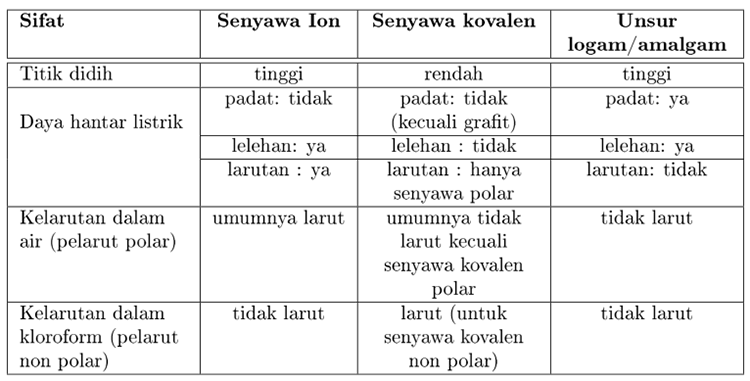
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College
![]()
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po

1 Senyawa Kovalen Polar Dan Non Polar Ppt Download
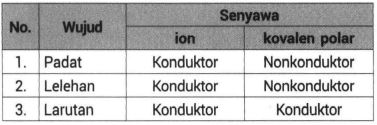
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po
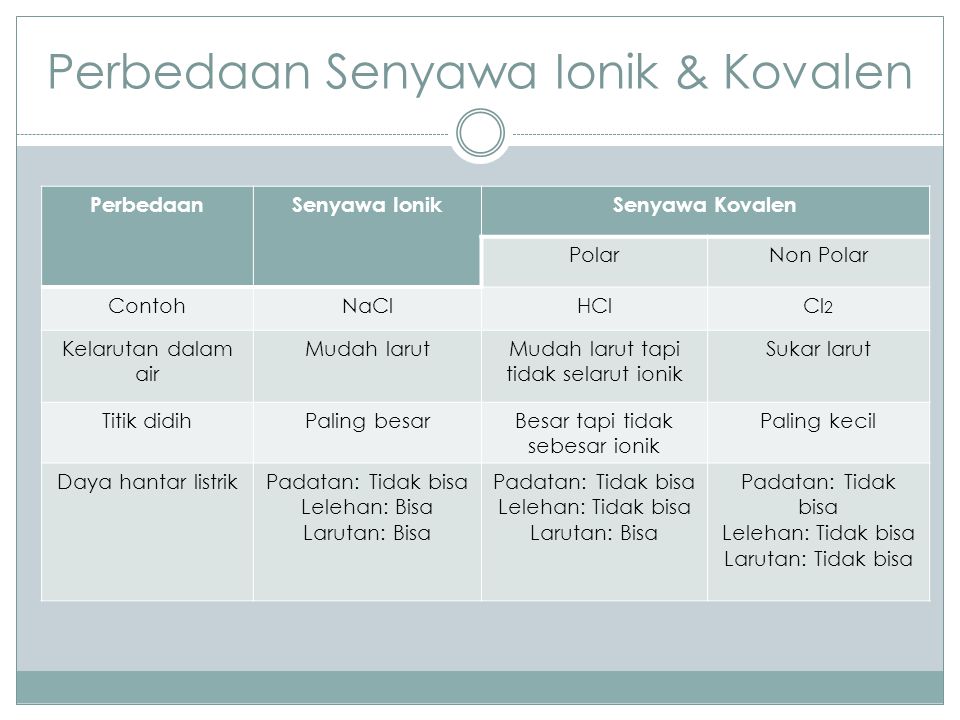
Ikatan Kimia Diusun Oleh Ppt Download

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Sebutkan 8 Perbedaan Senyawa Polar Dan Nonpolar Konsep Pentingnya Usaha Tiga Dua Satu

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya
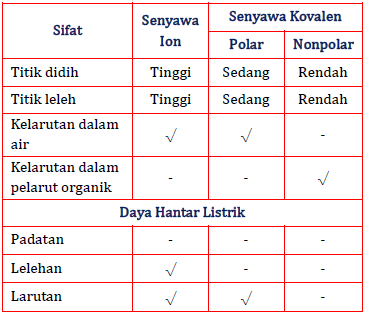
Perhatikan Data Sifat Fisik Dua Zat Berikut Je
Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya

Ciri Ciri Ikatan Ion Ikatan Kovalen Polar Dan Nonpolar Brainly Co Id
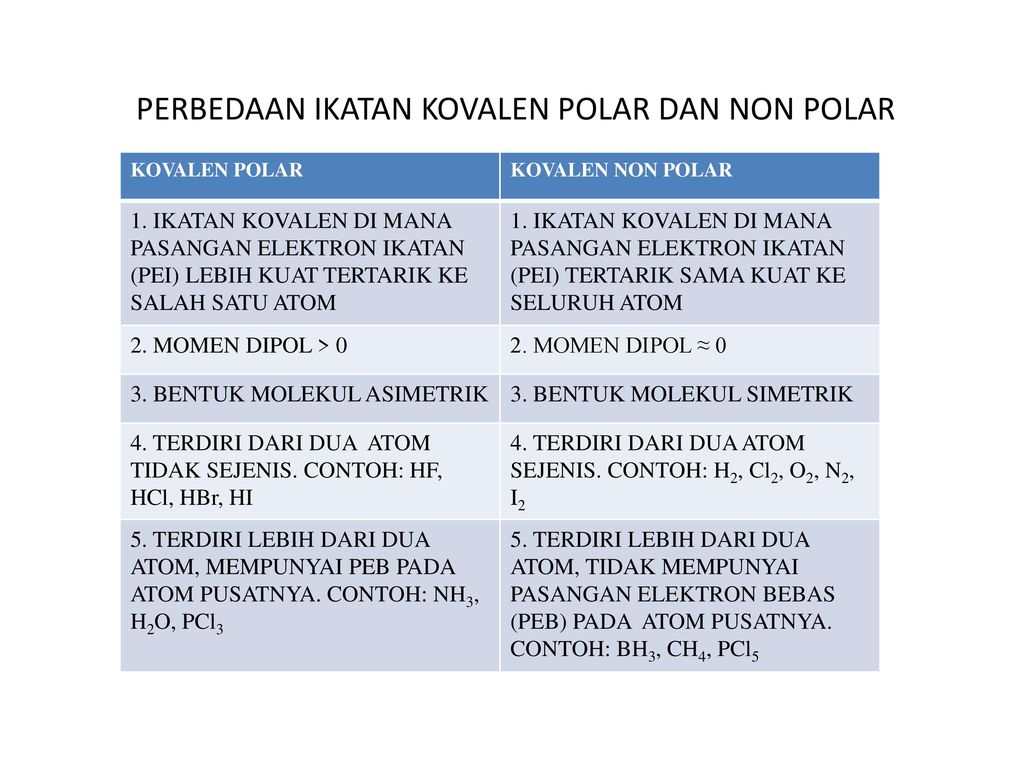
Perbedaan Ikatan Kovalen Polar Dan Non Polar Ppt Download

Sebutkan 8 Perbedaan Senyawa Polar Dan Nonpolar Konsep Pentingnya Usaha Tiga Dua Satu

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom

